1. Introduktion: Varför är Glykolysen Livsviktig?
Tänk på glykolysen som den absoluta grundbulten i cellens energimetabolism. Det är en uråldrig, universell process som sker i cytosolen i alla kroppens celler, från en nervcell i hjärnan till en röd blodkropp utan mitokondrier.
Huvudsyften:
- Snabb ATP-produktion: Glykolysen kan generera ATP snabbt, utan behov av syre. Detta är kritiskt vid t.ex. intensivt muskelarbete.
- Byggstenar för syntes: Intermediärerna (mellanprodukterna) i glykolysen är startpunkter för syntes av aminosyror, fetter och nukleotider.
- Förbereda för mer energi: Slutprodukten, pyruvat, är bränslet för citronsyracykeln och den oxidativa fosforyleringen, där den stora mängden ATP produceras.
Fysiologiskt Perspektiv: Blodsockernivån, eller glukoskoncentrationen i blodet, är strikt reglerad.
- Hypoglykemi (för lågt blodsocker): Hjärnan är nästan helt beroende av glukos. För låga nivåer leder till förvirring, kramper, medvetslöshet och i värsta fall bestående hjärnskador.
- Hyperglykemi (för högt blodsocker): Kroniskt höga nivåer är toxiskt. Det kan leda till glykosylering av proteiner (proteiner “sockras” och slutar fungera), vilket skadar blodkärl, nerver och organ. Detta är den centrala patofysiologin vid diabetes mellitus.
Den aeroba glykolysens netto-reaktion är:
Glukos+2 NAD++2 ADP+2 Pi→2 Pyruvat+2 NADH+2 H++2 ATP+2 H2O
2. Vägen in i Cellen: Glukostransportörer (GLUT & SGLT)
Innan glykolysen kan börja måste glukos ta sig in i cellen. Detta sker via två huvudfamiljer av transportproteiner.
- GLUT (Faciliterad diffusion): Dessa transportörer följer koncentrationsgradienten. De behöver inte energi, men de behöver en högre glukoskoncentration utanför cellen än inuti.
- SGLT (Natrium-glukos-kotransport): Dessa är sekundära aktiva transportörer som använder natriumgradienten (skapad av Na+/K+-pumpen) för att pumpa in glukos mot dess koncentrationsgradient. Detta är avgörande i tarmen (för att absorbera all glukos från maten) och i njurarna (för att återabsorbera all glukos från primärurinen).
Här är en mer detaljerad tabell över de viktigaste GLUT-transportörerna:
| Glukostransportör | Huvudsaklig Förekomst | Egenskaper och Fysiologisk Funktion | Klinisk Relevans |
| GLUT1 | Erytrocyter, blod-hjärnbarriären, foster-vävnad | Hög affinitet (lågt K_m). Säkerställer ett konstant basalt glukosupptag för livsviktiga vävnader, oberoende av insulinnivåer. | Sällsynta genetiska defekter i GLUT1 leder till allvarliga neurologiska sjukdomar p.g.a. energibrist i hjärnan. |
| GLUT2 | Lever, pankreas (β-celler), tunntarm, njure | Låg affinitet (högt K_m). Fungerar som en “glukossensor”. Transporterar glukos endast vid höga koncentrationer (efter måltid). I levern möjliggör den både upptag och frisättning av glukos. | Viktig för insulinfrisättning från pankreas. Polymorfismer kan vara associerade med diabetesrisk. |
| GLUT3 | Hjärnan (neuroner), placenta | Mycket hög affinitet (mycket lågt K_m). Garanterar att neuroner får glukos även vid låga blodsockernivåer. | |
| GLUT4 | Skelettmuskulatur, hjärtmuskulatur, fettvävnad | Insulinreglerad! Lagras i vesiklar inuti cellen. När insulin binder till sin receptor translokeras dessa vesiklar till cellmembranet, vilket dramatiskt ökar glukosupptaget. | Central mekanism för hur insulin sänker blodsockret. Insulinresistens (vid typ 2-diabetes) innebär att denna process är nedsatt. |
| GLUT5 | Tunntarmen, testiklar | Primär transportör för fruktos, inte glukos. | Fruktosmalabsorption kan uppstå vid nedsatt funktion. |
3. Glykolysens Tio Steg: En Detaljerad Genomgång
Glykolysen delas in i två faser:
- Energi-investeringsfasen (Steg 1-5): Cellen “betalar” med 2 ATP för att aktivera och klyva glukosmolekylen.
- Energi-avkastningsfasen (Steg 6-10): Cellen får tillbaka 4 ATP och 2 NADH. Nettoavkastningen är 2 ATP och 2 NADH.
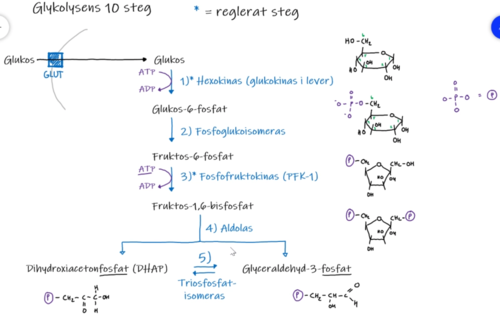
ENERGI-INVESTERINGSFASEN
Steg 1: Fosforylering av Glukos
- Reaktion: Glukos + ATP → Glukos-6-fosfat + ADP
- Enzym: Hexokinas (de flesta vävnader) eller Glukokinas (lever och pankreas)
- Fysiologi: Detta steg “fångar” glukosen inuti cellen. Fosfatgruppen är negativt laddad, vilket hindrar molekylen från att passera ut genom membranet via GLUT-transportörerna.
- Reglering & Reversibilitet:Irreversibelt. Detta är det första reglerande steget.
- Hexokinas: Har hög affinitet (lågt K_m) och hämmas av sin produkt, glukos-6-fosfat. Fungerar nära maxhastighet även vid låga glukosnivåer.
- Glukokinas: Har låg affinitet (högt K_m). Är inte mättat vid normala blodsockernivåer och hämmas inte av produkten. Detta gör att levern effektivt kan ta hand om stora mängder glukos efter en måltid för att lagra det som glykogen.
Steg 2: Isomerisering
- Reaktion: Glukos-6-fosfat ↔ Fruktos-6-fosfat
- Enzym: Fosfoglukos isomeras
- Fysiologi: Omlagring från en aldos (glukos) till en ketos (fruktos). Detta är en förberedelse för nästa fosforylering och klyvning.
- Reglering & Reversibilitet: Reversibelt och inte reglerat.
Steg 3: Den Andra Fosforyleringen – Det Viktigaste Steget!
- Reaktion: Fruktos-6-fosfat + ATP → Fruktos-1,6-bisfosfat + ADP
- Enzym: Fosfofruktokinas-1 (PFK-1)
- Fysiologi: Detta är det viktigaste, hastighetsbegränsande och engagerande (committed step) steget i hela glykolysen. När denna reaktion har skett, är molekylen låst till att genomgå resten av glykolysen.
- Reglering & Reversibilitet:Irreversibelt. Extremt komplext reglerat:
- Hämning (signalerar hög energi):
- ATP: Höga nivåer av ATP hämmar enzymet allosteriskt. Logiskt – om cellen har gott om energi behöver den inte köra glykolysen.
- Citrat: En intermediär från citronsyracykeln. Höga nivåer signalerar att det finns gott om bränsle för vidare bearbetning, så glykolysen kan sakta ner.
- Aktivering (signalerar låg energi):
- AMP: En mycket känslig indikator på låg energinivå. Aktiverar PFK-1 kraftigt.
- Fruktos-2,6-bisfosfat: Den mest potenta allosteriska aktivatorn. Denna molekyl produceras av enzymet PFK-2 som i sin tur styrs av insulin och glukagon.
- Insulin (högt blodsocker): Leder till defosforylering och aktivering av PFK-2 -> mer Fruktos-2,6-bisfosfat -> PFK-1 aktiveras -> Glykolysen körs.
- Glukagon (lågt blodsocker): Leder till fosforylering och inaktivering av PFK-2 -> mindre Fruktos-2,6-bisfosfat -> PFK-1 hämmas -> Glykolysen stannar av (och glukoneogenesen främjas).
- Hämning (signalerar hög energi):
Steg 4: Klyvning
- Reaktion: Fruktos-1,6-bisfosfat ↔ Dihydroxiacetonfosfat (DHAP) + Glyceraldehyd-3-fosfat (G3P)
- Enzym: Aldolas
- Fysiologi: Den 6-kolsmolekylen klyvs till två 3-kolsmolekyler.
- Reglering & Reversibilitet: Reversibelt och inte reglerat.
Steg 5: Isomerisering av triosfosfater
- Reaktion: Dihydroxiacetonfosfat (DHAP) ↔ Glyceraldehyd-3-fosfat (G3P)
- Enzym: Triosfosfat isomeras
- Fysiologi: Endast G3P kan fortsätta i glykolysen. Detta enzym omvandlar därför snabbt all DHAP till G3P. Från och med nu sker alltså alla efterföljande steg två gånger för varje ursprunglig glukosmolekyl.
- Reglering & Reversibilitet: Reversibelt och inte reglerat.
ENERGI-AVKASTNINGSFASEN (Alla steg x 2)
Steg 6: Oxidation och Fosforylering
- Reaktion: G3P + NAD⁺ + Pᵢ ↔ 1,3-Bisfosfoglycerat + NADH + H⁺
- Enzym: Glyceraldehyd-3-fosfat dehydrogenas
- Fysiologi: Det första energigenererande steget. En hög-energi fosfatbindning skapas och NADH bildas. NADH är en elektronbärare som senare kan generera ~2.5 ATP i den oxidativa fosforyleringen.
- Patofysiologi: Tillgången på NAD⁺ är begränsande. Om cellen inte kan återoxidera NADH till NAD⁺ (vilket kräver syre eller laktatbildning), stannar detta steg och hela glykolysen av.
Steg 7: Första ATP-produktionen (Substratnivåfosforylering)
- Reaktion: 1,3-Bisfosfoglycerat + ADP → 3-Fosfoglycerat + ATP
- Enzym: Fosfoglycerat kinas
- Fysiologi: Här skördas den första ATP-vinsten. Energin från hög-energi-fosfatbindningen överförs direkt till ADP för att bilda ATP. Detta kallas substratnivåfosforylering.
- Reglering & Reversibilitet: Reversibelt.
Steg 8: Omlagring av fosfatgruppen
- Reaktion: 3-Fosfoglycerat ↔ 2-Fosfoglycerat
- Enzym: Fosfoglycerat mutas
- Fysiologi: Flyttar fosfatgruppen för att förbereda molekylen för att skapa nästa hög-energi-intermediär.
- Reglering & Reversibilitet: Reversibelt.
Steg 9: Dehydrering
- Reaktion: 2-Fosfoglycerat ↔ Fosfoenolpyruvat (PEP) + H₂O
- Enzym: Enolas
- Fysiologi: Ett vatten tas bort, vilket skapar en mycket instabil och energirik enol-fosfatbindning i PEP.
- Reglering & Reversibilitet: Reversibelt.
Steg 10: Andra ATP-produktionen
- Reaktion: Fosfoenolpyruvat (PEP) + ADP → Pyruvat + ATP
- Enzym: Pyruvatkinas
- Fysiologi: Den andra substratnivåfosforyleringen, där den sista ATP-vinsten skördas.
- Reglering & Reversibilitet:Irreversibelt. Det tredje och sista reglerande steget.
- Aktivering: Fruktos-1,6-bisfosfat (från steg 3) aktiverar pyruvatkinas. Detta är ett exempel på feed-forward-aktivering – en tidig produkt i vägen signalerar att mer substrat är på väg, så det sista steget ska skynda på.
- Hämning:
- ATP och aminosyran Alanin (som syntetiseras från pyruvat) signalerar att det finns gott om energi och byggstenar.
- Hormonell (i levern): Glukagon -> PKA -> fosforylering och inaktivering av pyruvatkinas. Detta är avgörande för att förhindra att glykolys och glukoneogenes körs samtidigt.
- Klinisk Relevans: Pyruvatkinas-brist är den vanligaste enzymdefekten i glykolysen och en vanlig orsak till ärftlig hemolytisk anemi. Utan tillräckligt med ATP kan röda blodkroppar inte upprätthålla sin Na+/K+-pump, vilket leder till att de sväller och spricker (hemolys).
4. Pyruvatets Öde: Korsvägen i Metabolismen
Pyruvat är en central molekyl med flera möjliga öden beroende på celltyp och syretillgång:
- Aerob metabolism (syre finns): Pyruvat transporteras in i mitokondrien och omvandlas av pyruvatdehydrogenaskomplexet (PDH) till Acetyl-CoA. Acetyl-CoA går sedan in i citronsyracykeln för att producera stora mängder NADH och FADH₂, som driver den oxidativa fosforyleringen och genererar ~30-32 ATP per glukos.
- Anaerob metabolism (syre saknas): Pyruvat reduceras till Laktat i cytosolen.
- Anaplerotisk reaktion/Glukoneogenes: Pyruvat kan omvandlas till Oxalacetat av pyruvatkarboxylas. Detta fyller på citronsyracykeln eller fungerar som startpunkt för glukoneogenesen (nysyntes av glukos).
5. Anaerob Glykolys & Cori-cykeln
- Varför bildas laktat?I frånvaro av syre kan mitokondriens elektrontransportkedja inte återoxidera NADH till NAD⁺. Utan NAD⁺ skulle steg 6 i glykolysen stanna, och därmed all ATP-produktion. Reaktionen där pyruvat omvandlas till laktat av enzymet laktatdehydrogenas (LDH) konsumerar NADH och återbildar NAD⁺.$$$$$$\\text{Pyruvat} + \\text{NADH} + \\text{H}^+ \\leftrightarrow \\text{Laktat} + \\text{NAD}^+ $$$$$$Detta är en “nödlösning” för att tillåta glykolysen att fortsätta producera 2 ATP per glukos. Detta sker i t.ex. hårt arbetande muskler och i röda blodkroppar (som saknar mitokondrier).
- Laktatacidos:Om laktatproduktionen överstiger kroppens förmåga att metabolisera det (främst i levern), ansamlas det i blodet. Eftersom laktat (mjölksyra) är en syra, sänker detta blodets pH, vilket leder till en metabolisk acidos. Detta är ett allvarligt kliniskt tillstånd som ses vid chock, svår hypoxi och sepsis.
- Cori-cykeln:Detta är ett elegant samarbete mellan muskel och lever.
- I muskeln: Under anaerobt arbete omvandlas glukos till laktat.
- Transport: Laktat frisätts till blodet.
- I levern: Levern tar upp laktat från blodet och använder det för glukoneogenes för att syntetisera nytt glukos. Detta kostar 6 ATP i levern.
- Transport: Det nybildade glukoset frisätts till blodet och kan tas upp av muskeln igen.
6. Hormonell Reglering och Kliniska Aspekter
Den övergripande styrningen av glykolysen är hormonell, främst via insulin och glukagon.
| Hormon | Frisätts vid | Effekt på Blodsocker | Effekt på Glykolys | Mekanism (på nyckelenzymer) |
| Insulin | Högt blodsocker (efter måltid) | Sänker | Stimulerar | 1. Ökar transkription av Glukokinas, PFK-1, Pyruvatkinas. 2. Aktiverar PFK-2 (via defosforylering), vilket ökar F-2,6-BP och aktiverar PFK-1. 3. Främjar GLUT4-translokation till membranet i muskler/fett. |
| Glukagon | Lågt blodsocker (fasta) | Höjer | Hämmar | 1. Minskar transkription av nyckelenzymerna. 2. Inaktiverar PFK-2 (via fosforylering/PKA), vilket minskar F-2,6-BP och hämmar PFK-1. 3. Inaktiverar Pyruvatkinas (i levern, via fosforylering/PKA). |
Patofysiologi: Warburg-effekten i Cancerceller
Ett mycket viktigt koncept inom modern medicin. Många cancerceller uppvisar en dramatisk ökning av glukosupptag och glykolys, även i närvaro av syre (s.k. aerob glykolys). De omvandlar en stor del av glukos till laktat istället för att skicka det till mitokondrien.
- Varför? Teorin är att den snabba glykolysen, även om den är ineffektiv för ATP-produktion, genererar de byggstenar (intermediärer) som en snabbt delande cell behöver för att bygga nya celler.
- Klinisk användning: Denna egenskap utnyttjas i PET-scans (Positronemissionstomografi). Patienter injiceras med en radioaktiv glukosanalog (FDG). Tumörer med hög metabol aktivitet tar upp stora mängder FDG och “lyser upp” på bilderna, vilket gör att man kan lokalisera dem.
Sammanfattning och Tenta-tips
För att klara tentan, fokusera på följande:
- De tre irreversibla stegen (1, 3, 10): Känn till enzymerna (Hexokinas/Glukokinas, PFK-1, Pyruvatkinas) och deras specifika regulatorer.
- PFK-1 är kungen: Förstå varför det är det hastighetsbegränsande steget och hur ATP, AMP, citrat och framför allt Fruktos-2,6-bisfosfat styr det.
- Hormonell kontroll: Koppla ihop Insulin/Glukagon med PFK-2 och Pyruvatkinas (fosforylering/defosforylering).
- Anaerob vs. Aerob: Förstå varför laktat bildas (återbilda NAD⁺) och konsekvenserna (laktatacidos).
- Cori-cykeln: Beskriv samarbetet mellan muskel och lever.
- Kliniska kopplingar: Pyruvatkinasbrist (hemolytisk anemi), GLUT-transportörer (diabetes) och Warburg-effekten (cancer/PET-scan).
